2025. 04. 24. - 08:20
Mesterséges intelligencia és nyálteszt jelzi a kemoterápia kockázatát

Nyálteszt és mesterséges intelligencia képes a kemoterápia kockázatának előrejelzésére – adta hírül egy új, korai tanulmány. Mindez biztonságosabb, személyre szabottabb kezelést irányozhat elő.
Képes a mesterséges intelligencia nyálteszt bevonásával előrejelezni a kemoterápia kockázatát.
Egy új tanulmány korai eredményei arra utalnak, hogy az egyszerű nyálteszt és hatékony mesterséges intelligencia-algoritmusok segíthetnek az orvosoknak azonosítani azokat a rákos betegeket, akiknél nagy a rizikója a széles körben használt kemoterápiás gyógyszer súlyos mellékhatásainak.
A gyógyszer - az 5-fluorouracil (5-FU) - az 1950-es évek óta van használatban, így ez az egyik legrégebbi kemoterápiás szer. Továbbra is a rákkezelés sarokköve, a vastagbél-, mell-, fej- és nyakrák, hasnyálmirigy- és gyomorrák kemoterápiás kezeléseinek csaknem egyharmadában alkalmazzák.
Az 5-FU megzavarja a sejtek DNS előállítását és felhasználását. A rákos sejtek gyorsan osztódnak és folyamatosan másolniuk kell DNS-üket. A gyógyszer utánozza a DNS építőköveit és megakadályozza a folyamatot, megállítva a rákos sejtek növekedését. Olvasd el: Kemoterápiás dózis optimalizálását oldja meg a mesterséges intelligencia
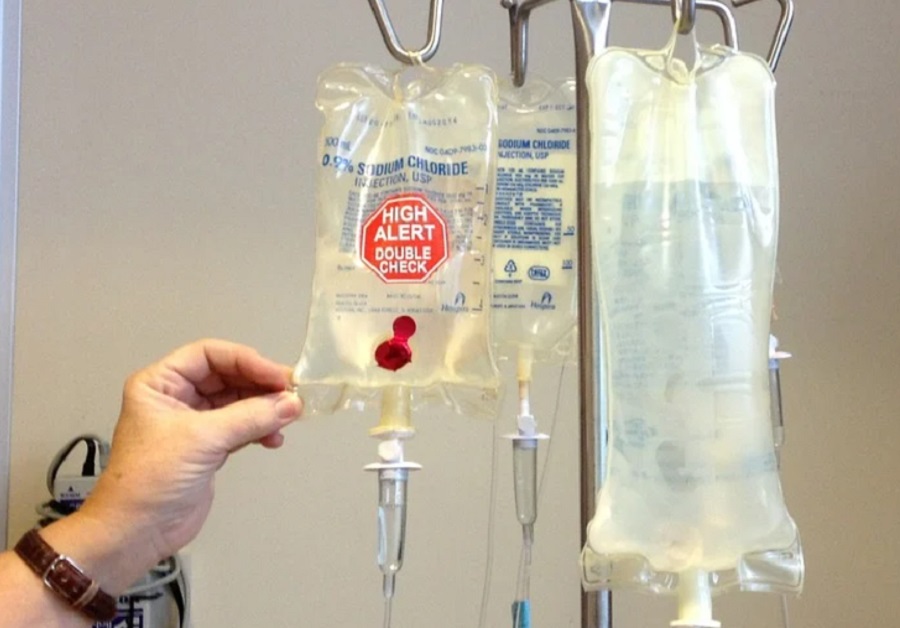
Mesterséges intelligencia és nyálteszt jelzi a kemoterápia kockázatát
Néhány beteg azonban olyan genetikai eltéréseket hordoz, amelyek meggátolják, hogy szervezetük megfelelően lebontsa a gyógyszert. Ilyen esetekben az 5-FU toxikus szintre emelkedhet, ami súlyos és néha életveszélyes szövődményeket okozhat.
Pontosabb kezelést ígér a mesterséges intelligencia-alapú megközelítés
Nagyjából minden harmadik embernek csökkent képessége van az 5-FU feldolgozására. Bár az amerikai Szövetségi Élelmiszer- és Gyógyszerügyi Hivatal javasolja a szűrést, nem alkalmazzák azt széles körben.
„Ez nemcsak az eredmények javításáról szól, hanem az életek megmentéséről” - mondta Carla Finkielstein, a VTC Fralin Orvosbiológiai Kutatóintézetének professzora, a tanulmány vezető szerzője.
„Évtizedek óta használják az 5-FU-t azzal a feltételezéssel, hogy mindenkinél ugyanúgy működik. Tudjuk azonban, hogy ez nem így van. Egyes személyek genetikailag fogékonyak erre a gyógyszerre. Megközelítésünk pontosabbá teszi azt a kezelést, amely évtizedek óta létezik, ám bizonyos páciensek számára még mindig komoly kockázatokat rejt magában” – tette hozzá a professzor.
A kutatás rávilágít az onkológusokkal és patológusokkal történő együttműködés kritikus szerepére, akiknek klinikai meglátásai hozzájárultak a kutatási irányhoz - jelezte Finkielstein. Olvasd el: Továbbterjed a mellrák? Az MI jobban tudja, mint a tesztek
Az előzetes eredményeket a projekt vezető kutatói, John Janiga és Dzenis Mahmutovic ismertették a 2025-ös ASCO Gastrointestinal Cancers Symposium rendezvényen. Kivonatként a Journal of Clinical Oncology folyóiratban is megjelentek, ami jelzi, hogy már van korai érdeklődés a tanulmány klinikai lehetőségei iránt.
Hogyan működik a mesterséges intelligencia-módszer?
A tudósok a DPYD nevű gén mutációira összpontosítottak, amely az 5-FU lebontásáért felelős enzimet termeli.
Kezdetben egészséges önkéntesek és rákos betegek DNS-ét elemezték annak megállapítására, hogy a nyálminták megbízhatóan kimutathatják-e az ismert DPYD mutációkat.
Az ismert változatokon túlmutató terjeszkedés érdekében a csapat később fejlett mesterséges intelligencia-eszközöket alkalmazott a 3D fehérjemodellezés mellett, hogy több ezer mintát kiértékeljen.
„A mesterséges intelligencia által vezérelt megközelítés segített a csapatnak felmérni a DPYD korábban fel nem ismert mutációinak szerkezeti és funkcionális hatását, feltárva azokat a potenciálisan káros változatokat, amelyeket a hagyományos módszerek esetleg kihagytak" - mondta Katherine Brown, a csapat vezető bioinformatikusa.
Több újonnan azonosított DPYD mutáció a vastagbélrákos pácienseknél várhatóan károsítja az 5-FU metabolizmust. Kettőt több előrejelző eszköz „kórokozónak” minősített és egy klinikai genetikai adatbázis ezt megerősítette.
Finkielstein – aki a Fralin Orvosbiológiai Kutatóintézet Virginia Tech Molekuláris Diagnosztikai Laboratóriumának vezetője – jelezte, hogy néhány magas kockázatú mutációt egészséges egyénekben is találtak, ami rávilágít a nyálalapú genetikai szűrés végrehajtásának szükségességére és megvalósíthatóságára a szélesebb populációs szintű kockázatértékelés érdekében.
„Ha korán meg tudjuk jelölni a magas kockázatú betegeket, személyre szabhatjuk kezelési terveiket, csökkenthetjük a kórházi kezelések számát és potenciálisan elkerülhetjük a végzetes szövődményeket" - mondta Finkielstein, a College of Science biológiai tudományok professzora is.
„Ez egy igazi előrelépés a rákkezelés biztonságosabbá, intelligensebbé és személyre szabottabbá tételében” – tette hozzá.
A korai eredmények kiterjeszthetik a jelenlegi genetikai vizsgálatokat, biztonságosabb, személyre szabottabb kemoterápiát előirányozva.
B.A.







